Wat je eigenlijk aan het doen bent is te vergelijken met een titratie van zoutzuur met natiumhydroxide. Hieronder zie je een afbeelding van zo'n titratiecurve.
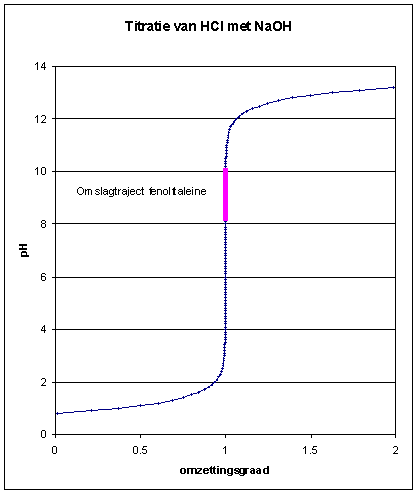
Op de opstaande as wordt de pH weergegeven en op de horizontale as het aantal mL NaOH dat je hebt toegevoegd.
Eerst en vooral is het belangrijk om te weten dat zoutzuur een sterk zuur is, bijgevolg zal dit onmiddellijk dissociëren in H
+ en Cl
- (HCl

H
+ + Cl
-). Verder kan je de pH van een oplossing berekenen door -log([H
+]) te nemen. Als gevolg van de volledige dissociatie is er in eerste instantie bijzonder veel H
+ aanwezig, dit verklaart de lage pH.
Verder is NaOH een sterke base welke ook volledig zal splitsen in Na
+ en OH
- (NaOH

Na
+ + OH
-). Wanneer je dus natriumhydroxide aan je zoutzuuroplossing gaat toevoegen ontstaat er een reactie tussen de H
+'jes en OH
- 'tjes waarbij water ontstaat (H
+ + OH
- 
H
2O). Vervolgens zijn er drie situaties:
- In het begin is er véél meer H+ aanwezig dan OH-, bijgevolg zullen alle OH--ionen wegreageren tot water en blijft er een groot deel H+ over. Je blijft dus met een lage pH zitten.
- Op een bepaald moment zal je precies evenveel OH--ionen toegevoegd hebben als er H+-ionen aanwezig waren. Na reactie blijft er dus geen H+ en OH- meer over, bijgevolg is de pH neutraal of m.a.w. gelijk aan 7.
- Wanneer je nu meer OH- gaat toevoegen dan H+ blijft na reactie enkele OH- over wat aanleiding geeft tot een hoge pH.
In een labo doe je zo'n titratie druppel per druppel,
dan kan je ongeveer een neutrale pH bekomen. Ik kan me voorstellen wanneer jij een scheut natriumhydroxide gaat toevoegen je onmiddellijk van links naar rechts op de grafiek springt

.
... en is er ook uit te rekenen hoeveel van het natrium hydroxide oplossing ik nodig ben per liter zoutzuur oplossing?
Je kan inderdaad uitrekenen hoeveel NaOH je moet toevoegen. Hiervoor zal je eens moeten uitzoeken wat de concentratie aan HCl is en of het gaat om massa procent (m-%) of volume procent (V-%).
Ik hoop dat ik de vraag overigens in het juiste subtopic staat. De meeste topic beschrijvingen waren voor mij aardig nieuw

Analytische chemie gaat meer over de analyse van moleculen of mengsels, je onderwerp past beter in anorganische chemie ik heb het dan ook even verplaatst.
"Success is the ability to go from one failure to another with no loss of enthusiasm" - Winston Churchill

 H+ + Cl-). Verder kan je de pH van een oplossing berekenen door -log([H+]) te nemen. Als gevolg van de volledige dissociatie is er in eerste instantie bijzonder veel H+ aanwezig, dit verklaart de lage pH.
H+ + Cl-). Verder kan je de pH van een oplossing berekenen door -log([H+]) te nemen. Als gevolg van de volledige dissociatie is er in eerste instantie bijzonder veel H+ aanwezig, dit verklaart de lage pH.