Tekenen structuurformule
Moderators: ArcherBarry, Fuzzwood
-
- Berichten: 226
Tekenen structuurformule
Kan iemand me helpen bij het tekenen van de structuurformule van Ca (OH)2?
Hoe moet ik de atomen t.o.v. elkaar plaatsen? In deze molecule zit zowel een covalente als ionbinding?? (Ca en O ->ionbinding en O en H covalente binding)
Alvast bedankt voor de hulp!!
Hoe moet ik de atomen t.o.v. elkaar plaatsen? In deze molecule zit zowel een covalente als ionbinding?? (Ca en O ->ionbinding en O en H covalente binding)
Alvast bedankt voor de hulp!!
- Berichten: 354
Re: Tekenen structuurformule
Het antwoord is ja.Kan iemand me helpen bij het tekenen van de structuurformule van Ca (OH)2?
Een toegift: H-O-Ca-O-H
-
- Berichten: 555
Re: Tekenen structuurformule
Om zoiets te tekenen, lis het belangrijk om op te merken dat er gewerkt wordt met OH-groepen.
Ze zullen dus samenblijven. Dan is de enige mogelijkheid die overblijft diegene waarbij Calcium centraal staat.
Ze zullen dus samenblijven. Dan is de enige mogelijkheid die overblijft diegene waarbij Calcium centraal staat.
- Pluimdrager
- Berichten: 2.722
Re: Tekenen structuurformule
Van calciumhydroxide kun je geen molecuulformule tekenen omdat het geen molecuul is.
Calciumhydroxide is een verbinding van een metaal en niet-metalen en daarom een zout.
Zouten zijn opgebouwd uit ionen, deze ionen zitten volgens een vast patroon in een kristalrooster verbonden door ionbingen. In dit geval Ca2+ -ionen en (OH)- ionen in de verhouding 1:2. Zouten hebben daarom een verhoudingsformule.
Ca(OH)2 is de verhoudingsformule van calciumhydroxide.
Van het (OH)- ion kun je wel de structuurformule geven: (O-H)- of (O:H)- .
De binding tussen het O- en het H-atoom is een covalente binding en je zou het ion daarom kunnen beschouwen als een stukje molecuul met lading -1.
Calciumhydroxide is een verbinding van een metaal en niet-metalen en daarom een zout.
Zouten zijn opgebouwd uit ionen, deze ionen zitten volgens een vast patroon in een kristalrooster verbonden door ionbingen. In dit geval Ca2+ -ionen en (OH)- ionen in de verhouding 1:2. Zouten hebben daarom een verhoudingsformule.
Ca(OH)2 is de verhoudingsformule van calciumhydroxide.
Van het (OH)- ion kun je wel de structuurformule geven: (O-H)- of (O:H)- .
De binding tussen het O- en het H-atoom is een covalente binding en je zou het ion daarom kunnen beschouwen als een stukje molecuul met lading -1.
-
- Berichten: 226
Re: Tekenen structuurformule
Maar in mijn cursus staat dat ik de structuurformulevia de Lewisnotatie van Ca(OH)2 moet tekenen??
- Pluimdrager
- Berichten: 2.722
Re: Tekenen structuurformule
Het hydroxyl-ion (OH-) bestaat uit twee atomen verbonden door een covalente binding, dus daarvan kun je wél de lewisstructuur weergeven. Probeer dit eens te doen.
Het hydroxyl-ion heeft de lading -1.
Waar denk je dat de lading zetelt? (Op het H-atoom of het O-atoom?)
Het hydroxyl-ion vormt een ionbinding met het calcium-ion.
Hoe denk je dat het hydroxyl-ion dan gericht is? Met de O of je H richting Ca2+ ?
Teken nu in de juiste richting een hydroxyl-ion links en een rechts van het Ca2+ -ion.
Vermoedelijk is dat de bedoeling van de vraagsteller in het boek.
Het hydroxyl-ion heeft de lading -1.
Waar denk je dat de lading zetelt? (Op het H-atoom of het O-atoom?)
Het hydroxyl-ion vormt een ionbinding met het calcium-ion.
Hoe denk je dat het hydroxyl-ion dan gericht is? Met de O of je H richting Ca2+ ?
Teken nu in de juiste richting een hydroxyl-ion links en een rechts van het Ca2+ -ion.
Vermoedelijk is dat de bedoeling van de vraagsteller in het boek.
-
- Berichten: 226
Re: Tekenen structuurformule
H-O <- Ca2+ -> O-H
Calcium staat 2 elektronen af 1 aan O links en 1 aan O rechts.
O heeft aan beide kanten 1 ongepaard elektron . Ca2+ geeft 1 elektron af aan O links .
Dat ongepaarde elektron maakt dan een binding met dat afgestane elektron van Ca (idem voor O rechts)
Klopt dit zo?
Calcium staat 2 elektronen af 1 aan O links en 1 aan O rechts.
O heeft aan beide kanten 1 ongepaard elektron . Ca2+ geeft 1 elektron af aan O links .
Dat ongepaarde elektron maakt dan een binding met dat afgestane elektron van Ca (idem voor O rechts)
Klopt dit zo?
- Pluimdrager
- Berichten: 2.722
Re: Tekenen structuurformule
Het klopt wel maar ik zou het toch wat anders tekenen. Zie bijlage.
-
- Berichten: 226
Re: Tekenen structuurformule
Merci voor de duidelijke tekening. Dit heb ik nu begrepen.
Ik heb soms nog moeilijk bij het bepalen van de polariteit van een molecule.
Ik ken de regeltjes wel (symmetrie (apolair) /assymetrie(polair)
Maar nu vb. in de verhoudingsformule Ca(OH)2.
Hoe kan je nu a.d.h.v. de tekening zien of deze polair is of niet??
Ik heb soms nog moeilijk bij het bepalen van de polariteit van een molecule.
Ik ken de regeltjes wel (symmetrie (apolair) /assymetrie(polair)
Maar nu vb. in de verhoudingsformule Ca(OH)2.
Hoe kan je nu a.d.h.v. de tekening zien of deze polair is of niet??
- Berichten: 7.390
Re: Tekenen structuurformule
We gaan uit van onderstaande afbeelding (thanks to Margriet).
Duid met een rode stip alle positieve ladingsdragers aan. Duid met groene stip alle negatieve ladingsdragers aan. Hoeveel rode heb je, hoeveel groene. Wat zie je?
Duid met een rode stip alle positieve ladingsdragers aan. Duid met groene stip alle negatieve ladingsdragers aan. Hoeveel rode heb je, hoeveel groene. Wat zie je?
"C++ : Where friends have access to your private members." Gavin Russell Baker.
-
- Berichten: 226
Re: Tekenen structuurformule
Je hebt 2 negatieve O en 2 positieve ladingen H . Ik denk dat het een apolaire molecule is
Heb je hier geen lineaire molecule?
Ik weet het niet meer goed...
Hoe zie ik nu of deze molecule een symmetrische structuur heeft want als de zwaartepunten van+ en - samenvallen zal de molecule toch ook apolair zijn.??
Heb je hier geen lineaire molecule?
Ik weet het niet meer goed...
Hoe zie ik nu of deze molecule een symmetrische structuur heeft want als de zwaartepunten van+ en - samenvallen zal de molecule toch ook apolair zijn.??
- Berichten: 7.390
Re: Tekenen structuurformule
De polariteit hangt af van het feit of dit een lineaire structuur is of een gebogen, zoals bij
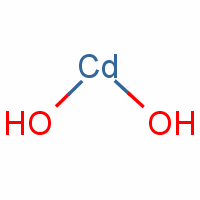
bijvoorbeeld. Is Ca(OH)2 lineair of gebogen?
Gezien de positie van Ca in het periodiek systeem zal je structuur erg gelijkaardig zijn aan die van Mg(OH)2. Dat kan je vaak toepassen: bestaan er gelijkaardige moleculen waar ik het wel van weet.

bijvoorbeeld. Is Ca(OH)2 lineair of gebogen?
Gezien de positie van Ca in het periodiek systeem zal je structuur erg gelijkaardig zijn aan die van Mg(OH)2. Dat kan je vaak toepassen: bestaan er gelijkaardige moleculen waar ik het wel van weet.
Verborgen inhoud
"C++ : Where friends have access to your private members." Gavin Russell Baker.
-
- Berichten: 226
Re: Tekenen structuurformule
Het centrale atoom (Ca) heeft toch geen valentie-elektronen meer. Heb je dan geen lineaire molecule?
- Berichten: 7.390
Re: Tekenen structuurformule
Om te beginnen: ik heb mijn bovenstaande post nog eens bekeken en nu ben ik er niet meer van overtuigd dat de afbeeldingen die erin staan wel kloppen - ook al vond ik ze op het net. Ik kom daar nog op terug.
Hoezo, het centrale Ca-atoom heeft toch geen valentie-elektronen meer? Die worden toch steeds gebruikt om een binding tot stand te brengen?
Wat jij bedoelt is dat er geen valentie-elektronenparen zijn die zorgen voor een buigingshoek zoals dat bij H2O wel het geval is. Dat klopt.
Hier zie je dat er twee valentie-elektronen zijn. Deze worden beiden gebruikt in de binding met onderstaande eenheid en zodoende zijn er geen elektronenparen die voor een buiging zorgen:
Bijgevolg lijkt je opmerking me correct. Ik kijk, zoals ik reeds zei, bovenstaande post nog eens na. Andere reacties zijn natuurlijk ook welkom
Hoezo, het centrale Ca-atoom heeft toch geen valentie-elektronen meer? Die worden toch steeds gebruikt om een binding tot stand te brengen?
Wat jij bedoelt is dat er geen valentie-elektronenparen zijn die zorgen voor een buigingshoek zoals dat bij H2O wel het geval is. Dat klopt.
Hier zie je dat er twee valentie-elektronen zijn. Deze worden beiden gebruikt in de binding met onderstaande eenheid en zodoende zijn er geen elektronenparen die voor een buiging zorgen:
Bijgevolg lijkt je opmerking me correct. Ik kijk, zoals ik reeds zei, bovenstaande post nog eens na. Andere reacties zijn natuurlijk ook welkom
"C++ : Where friends have access to your private members." Gavin Russell Baker.
-
- Berichten: 226
Re: Tekenen structuurformule
als er geen elektronenparen zijn die voor een buiging zorgen, dan heb je toch een lineaire molecule.
Het centrum van de partiële pos. en negatieve ladingen vallen dan toch samen. Dus is het dan een apolaire
molecule?
Het centrum van de partiële pos. en negatieve ladingen vallen dan toch samen. Dus is het dan een apolaire
molecule?
