Mijn vraag is nu, hoe dat eigenlijk juist zit met die polaire en apolaire kant bij isopropanol: welk een is polair en welk een is apolair? Een figuur van isopropanol vind je op http://zenstoves.net/Stoves.htm
Edit Mod(StrangeQuark): Ik heb even het plaatje er ook los bij gezet dat je niet zo lang hoeft te zoeken op de site.
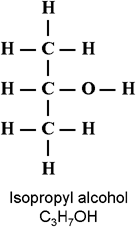
Dankje!