Bedankt voor je antwoord!
Ik wist eerlijk gezegd niet dat "mijn" reactie-mechanisme de niet-zuur-gekatalyseerde reactie voorstelde. Hoe verklaar je echter de H
+-opname in de volgende stap:
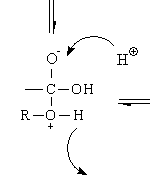
De H
+ die wordt opgenomen, is dat dan de H
+ die in diezelfde structuur wordt afgegeven? (De
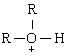
in die structuur reageert nl. zuur...)
Als "mijn" mechanisme inderdaad het niet-zuur-gekatalyseerde mechanisme zou moeten voorstellen, dan zouden er ook geen H
+-ionen in oplossing aanwezig zijn. Deze moet dan toch wel afkomstig zijn van die andere "groep" in het molecuul?
En ja, des te stabieler één der resonantiestructuren, des te groter zijn aandeel in de werkelijke structuur. Dit zou betekenen dat de eerste resonantiestructuur (van de drie getekende structuren) het grootste aandeel heeft in de werkelijke structuur, daaropvolgend de tweede en ten slotte de derde.
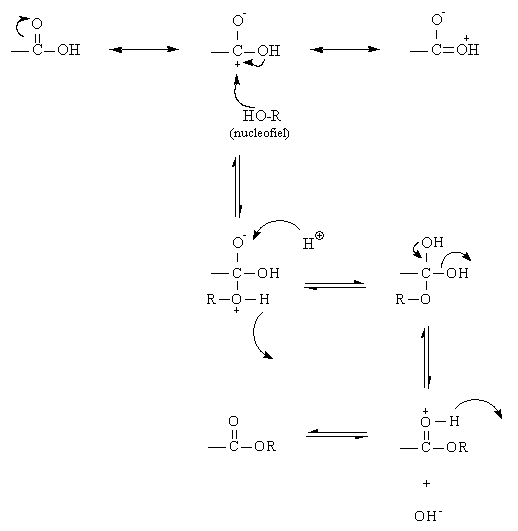

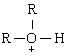 in die structuur reageert nl. zuur...)
in die structuur reageert nl. zuur...)