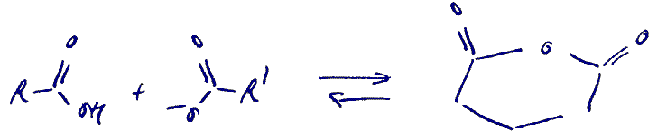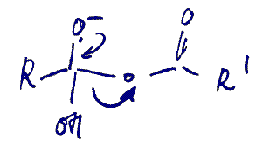De reactanten ontstaan hieruit:
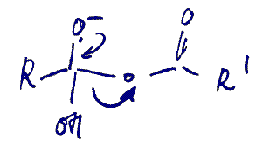
Het is uiteindelijk de bedoeling dat een molecuul pentaandizuur ontstaat uit een zuuranhydride. Dit doe je door een van de de carbonyl C-atomen van de anhydride te laten reageren met een H
2O-molecuul. (De л-binding van de carbonyl waaraan wordt geaddeert delocaliseert dan wel naar een vrij elektronenpaar op O waardoor een +-geladen carbocation ontstaat waar het H
2O-molecuul aan kan aanvallen.) Door de additie ontstaat een oxoniumgroep (-
+OH
2) en in een zuur-base-evenwicht verliest dit oxoniumgroep één H
+). Dan ontstaat bovenstaande structuur (in deze post). Het vrije elektronenpaar delocaliseert weer en
-O-(O=C)-R' wordt als leaving group eruit gestoten. Dan krijg je de twee producten die in mijn openingspost stonden. Vervolgens ontstaat daaruit blijkbaar een ring. :-s Hydrolyse van de ring levert uiteindelijk het gevraagde pentaandizuur.
Hoop dat het wat duidelijker is zo.