infra rood spectroscopie
Moderator: ArcherBarry
Forumregels
(Middelbare) school-achtige vragen naar het forum "Huiswerk en Practica" a.u.b.
Zie eerst de Huiswerkbijsluiter
(Middelbare) school-achtige vragen naar het forum "Huiswerk en Practica" a.u.b.
Zie eerst de Huiswerkbijsluiter
-
- Berichten: 11
infra rood spectroscopie
Ik zit in de knoei met IR spectroscopie. Er staat in mijn cursus uitgelegd dat het nodig is te werken met een assymetrische molecule dat een dipool bevat. Deze dipool moet gelijk trillen met de binding en met de electromagnetische straling. Als deze voorwaarde voldoen is de molecule gecshikt voor IR.
Waarom moet de molecule assymetrisch zijn en waarom is er een dipool nodig?
En wat wordt er bedoeld wanneer men zegt dat de dipool gelijk moet trillen met de chemische binding?
Iemand een idee?
bedankt!
grtjs
Waarom moet de molecule assymetrisch zijn en waarom is er een dipool nodig?
En wat wordt er bedoeld wanneer men zegt dat de dipool gelijk moet trillen met de chemische binding?
Iemand een idee?
bedankt!
grtjs
- Berichten: 217
Re: infra rood spectroscopie
Een molecule op zichzelf kan niet gezien worden als IR-actief of IR-inactief. Het gaat over de vibratiemodes van die molecule (zie ook gelijkaardige discussie ivm Raman-spectroscopie).
Hetzelfde voorbeeld als uit de link kan ik hier gebruiken. CO2 is een lineare molecule met verschillende vibratiesmodes. Eén hiervan is:
O<-C->O O->C<-O
Hierbij bewegen de zuurstoffen dus tegelijk weg van en terug naar het koolstofatoom. Het dipoolmoment gedurende deze vibratie verandert niet. Een andere:
O->C->O O<-C<-O
Zorgt er wél voor dat het dipoolmoment verandert. Nu is voor absorptie van IR-fotonen voor het exciteren van vibratiemodus een voorwaarde dat het dipoolmoment verandert, en zal de enkel de tweede vibratiemode aanleiding geven tot een signaal in IR. De achterliggende reden hiervoor is quantummechanisch bepaald, als je meer wil weten kan je googlen op "selection rules IR" bijvoorbeeld.
Ik denk dat het vooral belangrijk is dat je beseft dat IR (-en Raman) activiteit slaan op vibraties, en niet op moleculen.
Hetzelfde voorbeeld als uit de link kan ik hier gebruiken. CO2 is een lineare molecule met verschillende vibratiesmodes. Eén hiervan is:
O<-C->O O->C<-O
Hierbij bewegen de zuurstoffen dus tegelijk weg van en terug naar het koolstofatoom. Het dipoolmoment gedurende deze vibratie verandert niet. Een andere:
O->C->O O<-C<-O
Zorgt er wél voor dat het dipoolmoment verandert. Nu is voor absorptie van IR-fotonen voor het exciteren van vibratiemodus een voorwaarde dat het dipoolmoment verandert, en zal de enkel de tweede vibratiemode aanleiding geven tot een signaal in IR. De achterliggende reden hiervoor is quantummechanisch bepaald, als je meer wil weten kan je googlen op "selection rules IR" bijvoorbeeld.
Ik denk dat het vooral belangrijk is dat je beseft dat IR (-en Raman) activiteit slaan op vibraties, en niet op moleculen.
-
- Berichten: 11
Re: infra rood spectroscopie
Maar waarom veranderd in het ene geval dan die dipool en in het andere geval niet?
Ik heb die vorige discussie ook al gelezen maar ik ben er niet veel wijzer uit geworden vrees ik
Ik heb die vorige discussie ook al gelezen maar ik ben er niet veel wijzer uit geworden vrees ik
-
- Berichten: 2.337
Re: infra rood spectroscopie
Omdat niet meer aan de symmetrie is voldaan.
Waarom heeft tetrachloormethaan geen dipool en dichloormethaan wel? Dat is net hetzelfde als hier.
Waarom heeft tetrachloormethaan geen dipool en dichloormethaan wel? Dat is net hetzelfde als hier.
- Berichten: 217
Re: infra rood spectroscopie
Om het iets visueler voor te stellen, het dipoolmoment van deze twee momentopnames is hetzelfde:
O-----------C------------O en O---C---O
Gezien het een lineare molecule is. Je kan het zien als het uitrekken aan de ene kant wordt opgeheven door het evenveel uitrekken aan de andere kant.
O-----------C------------O en O---C---O
Gezien het een lineare molecule is. Je kan het zien als het uitrekken aan de ene kant wordt opgeheven door het evenveel uitrekken aan de andere kant.
-
- Berichten: 11
Re: infra rood spectroscopie
Ik vind het nog steeds moeilijk, maar het is toch al wat duidelijker..
Alleszins enorm bedankt!
Alleszins enorm bedankt!
-
- Berichten: 723
Re: infra rood spectroscopie
Als de trilling symmetrisch gebeurt dan verandert de dipool niet, een asymmetrische vibratie is wel IR actief.
Als er twee mensen, elk aan één van je armen trekt (dus één naar links en één naar rechts), met dezelfde kracht dan blijf je staan (symmetrisch). Als een van de twee harder trekt, geraak je uit balans (asymetrisch). De molecule moet als het ware uit balans worden gebracht.
Zo kan je het bekijken als je wil
Als er twee mensen, elk aan één van je armen trekt (dus één naar links en één naar rechts), met dezelfde kracht dan blijf je staan (symmetrisch). Als een van de twee harder trekt, geraak je uit balans (asymetrisch). De molecule moet als het ware uit balans worden gebracht.
Zo kan je het bekijken als je wil
- Berichten: 11.177
Re: infra rood spectroscopie
Misschien handig om te weten wat er nu gebeurt tijdens een IR opname. Bij het nemen ervan wordt een bepaald spectrum uitgezonden. Een detector registreert dat spectrum. Als er geen stof inzit, of wanneer de IR machine ingesteld is op een blanco en alleen de blanco zit in de houder, zul je een vlakke lijn krijgen.
Het apparaat werkt op basis van energie-opnames door de bindingen. Nu moet je weten dat een C-H binding met een andere frequentie trilt dan een C-C of een C-O binding. Alleen op die frequentie zal die binding IR-straling opnemen, dat resulteert in een daling van het teruggekaatste energieniveau. Dat zie je dus ook in het spectrum terug.
Nu moet je van frequenties weten dat die elkaar kunnen versterken of uitdoven. Dan krijg je dit effect:
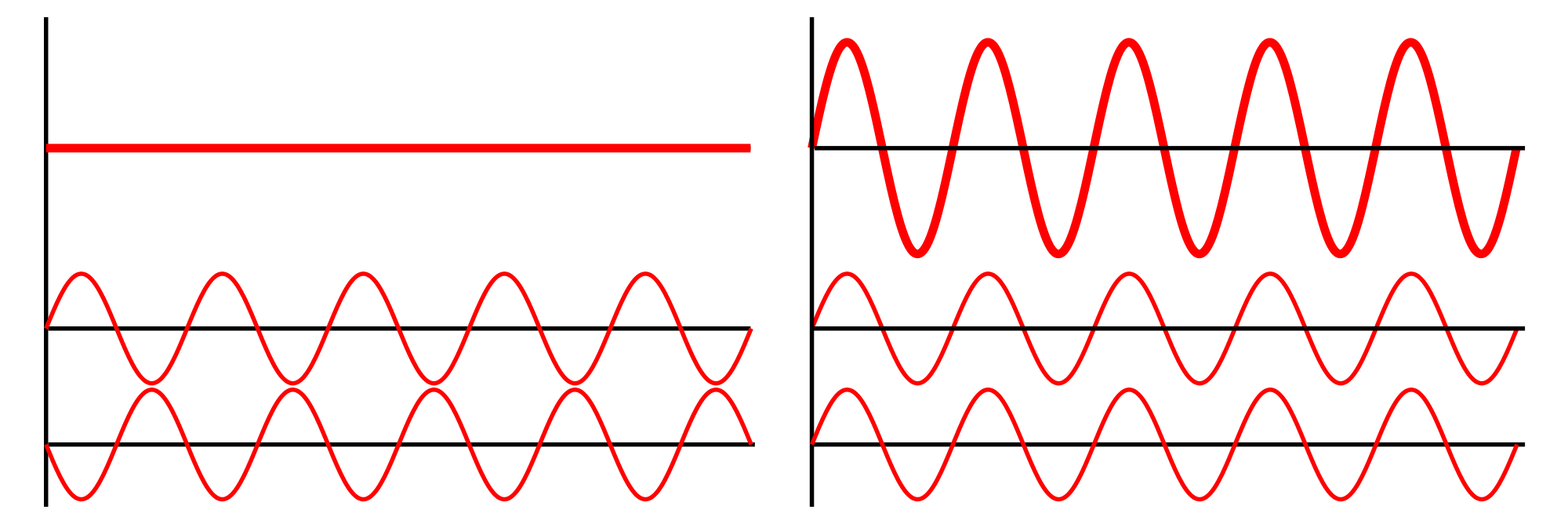
Bron: http://nl.wikipedia.org/wiki/Interferentie_%28natuurkunde%29
Het 2e geval, die met de vlakke lijn, is hetgeen er plaatsvindt bij een symmetrisch molecuul. Er is geen verandering van dipoolmoment, dus het molecuul "trilt" netto gezien niet (vlakke lijn) en er zal ook geen energieopname plaatsvinden. Geen energie opname, geen piek.
Het apparaat werkt op basis van energie-opnames door de bindingen. Nu moet je weten dat een C-H binding met een andere frequentie trilt dan een C-C of een C-O binding. Alleen op die frequentie zal die binding IR-straling opnemen, dat resulteert in een daling van het teruggekaatste energieniveau. Dat zie je dus ook in het spectrum terug.
Nu moet je van frequenties weten dat die elkaar kunnen versterken of uitdoven. Dan krijg je dit effect:

Bron: http://nl.wikipedia.org/wiki/Interferentie_%28natuurkunde%29
Het 2e geval, die met de vlakke lijn, is hetgeen er plaatsvindt bij een symmetrisch molecuul. Er is geen verandering van dipoolmoment, dus het molecuul "trilt" netto gezien niet (vlakke lijn) en er zal ook geen energieopname plaatsvinden. Geen energie opname, geen piek.
-
- Berichten: 11
Re: infra rood spectroscopie
Ik had het hier even niet in de gaten gehouden maar erg bedankt voor de uitleg, ik begrijp het nu toch al een pak beter.
Het enige waar ik dan nog een vraag bij stel is het dipoolmoment van C-C. Heeft dit een dipoolmoment want ik zou denken van niet...
Het enige waar ik dan nog een vraag bij stel is het dipoolmoment van C-C. Heeft dit een dipoolmoment want ik zou denken van niet...
- Berichten: 11.177
Re: infra rood spectroscopie
Nope, heeft het ook niet, wel als het dubbele of 3-dubbele bindingen heeft. Die hebben de neiging te resoneren als daar in het molecuul mogelijkheden voor bestaan. Resonantie --> asymmetrie --> piek 
-
- Berichten: 11
Re: infra rood spectroscopie
c=c heeft dus een dipool ? Dat begrijp ik niet... Zij trekken toch even hard aan de elektronen?
En als dit geen dipoolheeft... hoe kan dan dan gezien worden in een IR spectrum?
grtjs
En als dit geen dipoolheeft... hoe kan dan dan gezien worden in een IR spectrum?
grtjs
-
- Berichten: 2.337
Re: infra rood spectroscopie
Maar die elektronen van die dubbele binding zitten soms eens wat meer bij de ene of bij de andere -----> assymetrie---->piek
-
- Berichten: 11
Re: infra rood spectroscopie
Achzo! Goed, het begint allemaal wat op te klaren 
Bedankt allemaal voor de uitleg!
Bedankt allemaal voor de uitleg!