[scheikunde] Titratie zwak zuur
Moderators: ArcherBarry, Fuzzwood
-
- Berichten: 5
[scheikunde] Titratie zwak zuur
Hallo allemaal,
Ik kwam de volgende vraag tegen, en kon niet op het antwoord uitkomen:
tijdens de titratie is er sprake geweest van een bufferoplossing. geef aan op welk moment tijdens de titratie er sprake was van een buffer.
deze titratie is uitgevoerd door middel van een onbekend zwak zuur dat getitreerd werd met natronloog. de indicator die gebruikt is fenolftaleine.
voor de mensen die niet weten wat een bufferoplossing is, maar toch graag willen helpen:
De buffer zoals die wordt genoemd zorgt ervoor dat de pH na het toevoegen van een base of zuur constant blijft. Een buffer bestaat in de scheikunde uit een waterige oplossing van 2 stoffen die in evenwicht zijn en een bepaalde pH hebben. De pH staat al vast van te voren.
Ik zelf was aan het denken, aan het omslagpunt, maar is dit goed, en zo ja, waarom? ( mijn gedachte was dat het tijdens de titratie alleenmaar om het omslagpunt draait, endus...)
alvast bedankt
Ik kwam de volgende vraag tegen, en kon niet op het antwoord uitkomen:
tijdens de titratie is er sprake geweest van een bufferoplossing. geef aan op welk moment tijdens de titratie er sprake was van een buffer.
deze titratie is uitgevoerd door middel van een onbekend zwak zuur dat getitreerd werd met natronloog. de indicator die gebruikt is fenolftaleine.
voor de mensen die niet weten wat een bufferoplossing is, maar toch graag willen helpen:
De buffer zoals die wordt genoemd zorgt ervoor dat de pH na het toevoegen van een base of zuur constant blijft. Een buffer bestaat in de scheikunde uit een waterige oplossing van 2 stoffen die in evenwicht zijn en een bepaalde pH hebben. De pH staat al vast van te voren.
Ik zelf was aan het denken, aan het omslagpunt, maar is dit goed, en zo ja, waarom? ( mijn gedachte was dat het tijdens de titratie alleenmaar om het omslagpunt draait, endus...)
alvast bedankt
-
- Berichten: 24
Re: [scheikunde] Titratie zwak zuur
Hallo!
een buffer bij het omslagpunt?
bedenk nog eens goed wat er gebeurd bij titreren bij zo'n omslagpunt, en vooral waarom het zo makkelijk mis gaat.
een buffer bij het omslagpunt?
bedenk nog eens goed wat er gebeurd bij titreren bij zo'n omslagpunt, en vooral waarom het zo makkelijk mis gaat.
-
- Berichten: 5
Re: [scheikunde] Titratie zwak zuur
mag ik vragen wat het dan wel moet zijn?
ikzelf loop nu helemaal vast.
ikzelf loop nu helemaal vast.
-
- Berichten: 2
Re: [scheikunde] Titratie zwak zuur
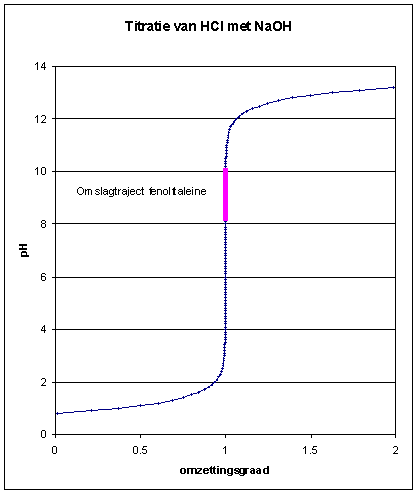
het eerste gedeelte van de titratie tot iets voor het equavilentie punt gedraagt zich als een buffer, als je de PH uitzet tegenover de concentratie toegevoegde NaOH krijg je een S-curve, het is dan duidelijk te zien waar de buffer zich bevindt.

- Berichten: 11.177
Re: [scheikunde] Titratie zwak zuur
Het is echter niet de bedoeling dat je zomaar het antwoord weggeeft in de huiswerk en toetsen-sectie. Hier leert de topicstarter niet echt wat van.
- Berichten: 2.455
Re: [scheikunde] Titratie zwak zuur
daarbij ga je bij het voorbeeld in de tekening geen buffer zien, meer "een pH die niet zo snel stijgt als bij het equivalentiepunt".
This is weird as hell. I approve.