[natuurkunde] atoomstructuur en bindingsenergie
Moderators: ArcherBarry, Fuzzwood
-
- Berichten: 15
atoomstructuur en bindingsenergie
Ik zit met 1 vraag waar ik totaal niet uit kom.
Barium. atoomnummer 56. 2 valentie elektronen. m=137 g.mol-1, body centered cubic-structuur
a) Laat zien dat er 4 atoom bindingen zijn (m.b.v. coördinatiegetal)
De smeltwarmte L = 7,75 kJ.mol-1
b) Bereken de bindingsenergie
Barium. atoomnummer 56. 2 valentie elektronen. m=137 g.mol-1, body centered cubic-structuur
a) Laat zien dat er 4 atoom bindingen zijn (m.b.v. coördinatiegetal)
De smeltwarmte L = 7,75 kJ.mol-1
b) Bereken de bindingsenergie
- Berichten: 2.455
Re: atoomstructuur en bindingsenergie
Luchtkwaliteit schreef: ↑wo 26 jun 2013, 17:15
Laat zien dat er 4 atoom bindingen zijn (m.b.v. coördinatiegetal)
ik neem aan dat men "per atoom" bedoelt. De eerste stap is: met hoeveel atomen is elk atoom gebonden in een bcc-structuur? Weet je wat dat is?
This is weird as hell. I approve.
-
- Berichten: 15
Re: atoomstructuur en bindingsenergie
Op de hoekpunten 4, in het midden 8. In totaal zouden dit dan 2 atomen zijn: de op de hoekpunten gelegen behoren maar voor 1/8 tot deze cel.
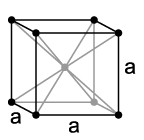
Plaatje uit Wikipedia.

Plaatje uit Wikipedia.
- Berichten: 10.561
Re: atoomstructuur en bindingsenergie
Die redenering kan ik niet helemaal volgen, waarom 4 op de hoekpunten en in het midden 8?
Bedenk dat dit een eenheidscel is in een repeterende structuur.
Wat is dus het coördinatiegetal? En uit hoeveel atomen bestaat een eenheidscel?
Bedenk dat dit een eenheidscel is in een repeterende structuur.
Wat is dus het coördinatiegetal? En uit hoeveel atomen bestaat een eenheidscel?
Cetero censeo Senseo non esse bibendum
-
- Berichten: 15
Re: atoomstructuur en bindingsenergie
Dus je moet het als geheel bekijken en niet per eenheidscel? Dan zijn het 8 bindingen per atoom. En 2 atomen per eenheidscel. Dan is 8/2=4. Maar hier zie ik niet in waarom dit logisch is om te doen.
- Berichten: 2.455
Re: atoomstructuur en bindingsenergie
een eenheidscel is een stukje uit een "oneindige" structuur. Bij de bcc-structuur zit je dus met één atoom "in het midden" van de eenheidscel. Maar dat geldt ook voor elk ander atoom: elk atoom is omringd door 8 buren, op de hoekpunten van een kubus. In de weergave van de eenheidscel beperk je jezelf tot het minimum aan getekende atomen om de globale structuur te schetsen. Deze globale structuur is hier: elk atoom zit in het midden van kubus, omringd door 8 buren op de hoekpunten.Luchtkwaliteit schreef: ↑do 27 jun 2013, 10:33
Dus je moet het als geheel bekijken en niet per eenheidscel?
Wat je hier dus moet meenemen (voor de opdracht): elk atoom heeft 8 buren/8 bindingen. Nu gegeven zij een rooster met N (=veel) atomen, hoeveel onderlinge bindingen zijn er dan?
This is weird as hell. I approve.
- Berichten: 2.455
Re: atoomstructuur en bindingsenergie
We doen een stap terug:
Je hebt één molecule, zeg, H2, dus H---H. Elke H is gebonden met één andere H: dus elke H heeft één binding. Hoeveel bindingen heb je in totaal, per H?
Je hebt één molecule, zeg, H2, dus H---H. Elke H is gebonden met één andere H: dus elke H heeft één binding. Hoeveel bindingen heb je in totaal, per H?
This is weird as hell. I approve.
-
- Berichten: 15
Re: atoomstructuur en bindingsenergie
Het coordinatiegetal is dus 8? Omdat bindingen altijd door 2 atomen gedeeld zijn zijn er 4 atoom-bindingen?
- Berichten: 2.455
Re: atoomstructuur en bindingsenergie
ja, en er zijn vier atoombindingen / atoom. Kan je dat volgen?
Hoe zou je nu b) kunnen oplossen? Ideeën?
Hoe zou je nu b) kunnen oplossen? Ideeën?
This is weird as hell. I approve.
-
- Berichten: 15
Re: atoomstructuur en bindingsenergie
Aantal atoombindingen is dus onafhankelijk van de stof, wordt puur bepaald door de structuur: voor bcc 4 en voor fcc zou dit dan 6 zijn?
Is hetgeen vermeld in mijn vorige reactie ook het bewijs dat het zo is? Of moet dit toch anders geformuleerd worden?
Voor de bindingsenergie. Eerst weten hoeveel mol je hebt zou ik zeggen. We weten 137 g/mol en L=7,75 kJ/mol. En verder?
Is hetgeen vermeld in mijn vorige reactie ook het bewijs dat het zo is? Of moet dit toch anders geformuleerd worden?
Voor de bindingsenergie. Eerst weten hoeveel mol je hebt zou ik zeggen. We weten 137 g/mol en L=7,75 kJ/mol. En verder?
- Berichten: 10.561
Re: atoomstructuur en bindingsenergie
Berekenen hoeveel mol je hebt is altijd een goede stap in chemische berekeningen.
Met die molmassa kun je niet zoveel, want er is nergens een massa gegeven.
Waar het om gaat is: je hebt net wat dingen beredeneerd die gelden voor een (1) atoom.
Maar wat je beredeneert voor 1 atoom, geldt net zo goed voor 1 mol atomen.
Het gaat dus uiteindelijk om het omrekenen van iets wat geldt voor 1 atoom naar iets wat geldt voor 1 mol atomen (per mol dus), of andersom.
De vraag is nu, wat moet er gebeuren bij smelten, en hoe is dat gerelateerd aan de gegevens die je hebt gekregen en aan hetgeen wat je in de eerste stappen hebt afgeleid?
Met die molmassa kun je niet zoveel, want er is nergens een massa gegeven.
Waar het om gaat is: je hebt net wat dingen beredeneerd die gelden voor een (1) atoom.
Maar wat je beredeneert voor 1 atoom, geldt net zo goed voor 1 mol atomen.
Het gaat dus uiteindelijk om het omrekenen van iets wat geldt voor 1 atoom naar iets wat geldt voor 1 mol atomen (per mol dus), of andersom.
De vraag is nu, wat moet er gebeuren bij smelten, en hoe is dat gerelateerd aan de gegevens die je hebt gekregen en aan hetgeen wat je in de eerste stappen hebt afgeleid?
Cetero censeo Senseo non esse bibendum
-
- Berichten: 15
Re: atoomstructuur en bindingsenergie
Er moet energie in om te smelten ofwel de bindingen moeten verbroken worden. Aangezien er 4 atoombindingen zijn wordt dit dan simpelweg 7,75/4= 1,94 kJ?
- Berichten: 10.561
Re: atoomstructuur en bindingsenergie
zijn er 4 bindingen per mol?
Cetero censeo Senseo non esse bibendum