Voor een po moeten we proberen de concentratie fosforzuur van cola te bepalen middels een neerslagreactie van het fosfaation en de bepaling van de daarbij vrijkomende H+ ionen.
Ik weet alleen niet hoe ik dit zou kunnen doen.
De gegevens die we erbij hebben gekregen zijn de reacties die achterelkaar plaatsvinden als je natronloog bij fosforzuur toevoegt:
H3PO4 + OHˉ ® H2PO4ˉ + H2O
H2PO4ˉ + OHˉ ® HPO42ˉ + H2O
HPO42ˉ + OHˉ ® PO43ˉ + H2O
Op wikipedia vond ik verder dit:
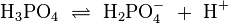


Ik dacht zelf om magnesiumchloride toe te voegen bij het fosforzuur zodat het fosfaation neerslaat met het magnesium en hierdoor dus magnesiumfosfaat ontstaat.
Vervolgens ga ik de cola waarin magnesiumchloride is gedaan, titreren met natronloog om zo de concentratie van het fosforzuur te weten kan komen.
Is dit een goede manier?
Ook vraag ik me af waarom het uberhaupt nodig is om het fosfaation eerste te laten neerslan met iets en dan pas titreren en waarom je niet de cola meteen kan titreren om zo het fosforzuurgehalte te bepalen.