voip4341 schreef: ↑ma 25 mar 2013, 19:15
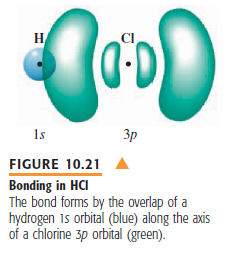
Dus we kunnen de halogenen gekoppeld aan een H zien als een uitzondering. Zijn er misschien nog andere uitzonderingen Typhoner?
Bijna alles is een uitzondering. De theorie van hybridisatie werkt in feite alleen voor C-atomen, en een beetje voor N-atomen. Voor O wordt het soms al lastig, zoals je hebt gezien, en voor alle andere elementen ook.
Neem bijvoorbeeld het H
2S molecuul. De bindingshoek is daar ongeveer 90 graden, en zeker geen 109.nogwat zoals hybridisatie zou voorspellen. Maar ook bij H
2O gaat het al fout. De hoek is daar 105 graden, maar misschien nog wel belangrijker: de theorie van hybridisatie suggereert dat er 2 "lobben" zijn voor de 2 vrije elektronenparen. Dan zou de negatieve lading in een H
2O molecuul, of in ieder geval een groot deel daarvan, zich moeten bevinden in 2 afzonderlijke lobben, en dat is zeker niet het geval.
Maar om terug te komen op het toepassen van hybridisatie: Ook al is het fout, je kunt het nog steeds toepassen. Er worden namelijk ook een heleboel dingen
wel goed mee verklaard. Je kunt het dus ook toepassen op andere atomen dan het centrale atoom, en ook als het om andere elementen dan C en N gaat.