Warmtecapaciteit verzadigde lucht
Moderator: physicalattraction
Forumregels
(Middelbare) school-achtige vragen naar het forum "Huiswerk en Practica" a.u.b.
Zie eerst de Huiswerkbijsluiter
(Middelbare) school-achtige vragen naar het forum "Huiswerk en Practica" a.u.b.
Zie eerst de Huiswerkbijsluiter
- Berichten: 3.135
Warmtecapaciteit verzadigde lucht
Weet iemand de warmtecapaciteit van met waterdamp verzadigde lucht, bij 1 atmosfeer, en bij een temperatuur van 33, 35, 37 en 39 graden Celsius?
Bij voorbaat dank!
Bij voorbaat dank!
Heb je interesse in journalistiek? Wij zoeken versterking! Speurwerk, deel van het team, meer weten: klik.
- Moderator
- Berichten: 51.282
Re: Warmtecapaciteit verzadigde lucht
Ik ben bijna geneigd te zeggen: a difference that makes no difference is no difference.
En daarmee heel benieuwd waarvoor je dát nodig hebt. Het gaat om temperaturen rondom de lichaamstemperatuur zo te zien. Uitademingslucht?
En daarmee heel benieuwd waarvoor je dát nodig hebt. Het gaat om temperaturen rondom de lichaamstemperatuur zo te zien. Uitademingslucht?
ALS WIJ JE GEHOLPEN HEBBEN...
help ons dan eiwitten vouwen, en help mee ziekten als kanker en zo te bestrijden in de vrije tijd van je chip...
http://www.wetenscha...showtopic=59270
help ons dan eiwitten vouwen, en help mee ziekten als kanker en zo te bestrijden in de vrije tijd van je chip...
http://www.wetenscha...showtopic=59270
- Berichten: 3.135
Re: Warmtecapaciteit verzadigde lucht
Het gaat om warmteoverdracht. Vind je het goed als ik niet verder in detail ga? Het gaat om een uitvinding pi.gif
Ik wil het volgende kunnen berekenen:
Als ik één kuub lucht door water van 35 graden Celsius leidt, (die dan verzadigd is naar ik aanneem), en vervolgens tegen een plaat laat afkoelen die een temperatuur heeft van 11 graden Celsius, hoeveel energie heb ik dan overgedragen?
Dezelfde vraag, maar dan als het water niet 35 graden is, maar 33, of 37 of 39.
Ik wil het volgende kunnen berekenen:
Als ik één kuub lucht door water van 35 graden Celsius leidt, (die dan verzadigd is naar ik aanneem), en vervolgens tegen een plaat laat afkoelen die een temperatuur heeft van 11 graden Celsius, hoeveel energie heb ik dan overgedragen?
Dezelfde vraag, maar dan als het water niet 35 graden is, maar 33, of 37 of 39.
Heb je interesse in journalistiek? Wij zoeken versterking! Speurwerk, deel van het team, meer weten: klik.
- Moderator
- Berichten: 51.282
Re: Warmtecapaciteit verzadigde lucht
http://www.natmus.dk/cons/tp/atmcalc/atmoclc1.htm
Die lucht koel je af tot 11°C, bij die temperatuur kun je ook de enthalpie van de verzadigde lucht berekenen.
de maximale g (dwz het maximale waterdampgehalte in kg per kg droge lucht bij de temperaturen die je interesseren) kun je vinden in Mollier-diagrammen (als je er kunt vinden die tot de 40°C gaan, kost wat moeite) of je kunt ze berekenen volgens een empirische formule op dezelfde site. Lang geleden dat ik dat gedaan heb, dat is héél diep weggezakt.Thermal properties of damp air
The heat content, usually called the enthalpy, of air rises with increasing water content. This hidden heat, called latent heat by air conditioning engineers, has to be supplied or removed in order to change the relative humidity of air, even at a constant temperature. This is relevant to conservators. The transfer of heat from an air stream to a wet surface, which releases water vapour to the air stream at the same time as it cools it, is the basis for psychrometry and many other microclimatic phenomena. Control of heat transfer can be used to control the drying and wetting of materials during conservation treatment.
The enthalpy of dry air is not known. Air at zero degrees celsius is defined to have zero enthalpy. The enthalpy, in kJ/kg, at any temperature, t, between 0 and 60C is approximately:
h = 1.007t - 0.026 below zero: h = 1.005t
The enthalpy of liquid water is also defined to be zero at zero degrees celsius. To turn liquid water to vapour at the same temperature requires a very considerable amount of heat energy: 2501 kJ/kg at 0C
At temperature t the heat content of water vapour is:
hw = 2501 + 1.84t
Notice that water vapour, once generated, also requires more heat than dry air to raise its temperature further: 1.84 kJ/kg.C against about 1 kJ/kg.C for dry air.
The enthalpy of moist air, in kJ/kg, is therefore:
h = (1.007*t - 0.026) + g*(2501 + 1.84*t)
g is the water content in kg/kg of dry air
Die lucht koel je af tot 11°C, bij die temperatuur kun je ook de enthalpie van de verzadigde lucht berekenen.
ALS WIJ JE GEHOLPEN HEBBEN...
help ons dan eiwitten vouwen, en help mee ziekten als kanker en zo te bestrijden in de vrije tijd van je chip...
http://www.wetenscha...showtopic=59270
help ons dan eiwitten vouwen, en help mee ziekten als kanker en zo te bestrijden in de vrije tijd van je chip...
http://www.wetenscha...showtopic=59270
- Moderator
- Berichten: 51.282
Re: Warmtecapaciteit verzadigde lucht
Bedenk me juist dat je die enthalpie ook rechtstreeks in het mollier-diagram kunt aflezen.... pi.gif
ALS WIJ JE GEHOLPEN HEBBEN...
help ons dan eiwitten vouwen, en help mee ziekten als kanker en zo te bestrijden in de vrije tijd van je chip...
http://www.wetenscha...showtopic=59270
help ons dan eiwitten vouwen, en help mee ziekten als kanker en zo te bestrijden in de vrije tijd van je chip...
http://www.wetenscha...showtopic=59270
- Berichten: 3.135
Re: Warmtecapaciteit verzadigde lucht
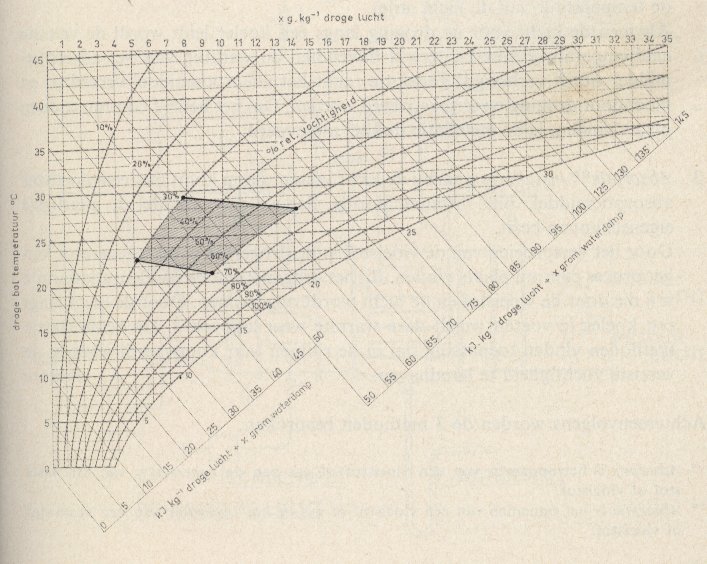
Lees ik de tabel goed?
Bij 11 graden Celsius: g = 8 [gram/kg] = 0,008 [kg/kg]
Bij 35 graden Celsius: g = 37 [gram/kg] = 0,037 [kg/kg]
Als ik dat dan invul in die formule voor enthalpie: h = (1.007*t - 0.026) + g*(2501 + 1.84*t)
Dan krijg ik bij 11 graden Celsius: h = 31 [kJ/kg]
En bij 35 graden Celsius: h = 130 [kJ/kg]

Heb ik het goed als ik denk dat voor iedere kilogram verzadigde lucht van 35 graden Celsius die wordt verplaatst en afkoelt en condenseert op een plaat van 11 graden Celsius, er 130 -31 = 99 [kJ] worden overgedragen?
Heb je interesse in journalistiek? Wij zoeken versterking! Speurwerk, deel van het team, meer weten: klik.
- Moderator
- Berichten: 51.282
Re: Warmtecapaciteit verzadigde lucht
Dat is wel de grote lijn ja. Ik weet alleen niet meer waar nou de details zitten. In je diagram staat óók een enthalpieschaal. Voor verzadigde lucht van 11°C komt die aardig overeen met wat je berekent, voor die 35°C komt die toch dichter in de buurt van de 145 kJ/kg ipv 130 kJ/kg.
Ik zou je niet durven zeggen waar dat verschil vandaan komt.
Ik zou je niet durven zeggen waar dat verschil vandaan komt.
ALS WIJ JE GEHOLPEN HEBBEN...
help ons dan eiwitten vouwen, en help mee ziekten als kanker en zo te bestrijden in de vrije tijd van je chip...
http://www.wetenscha...showtopic=59270
help ons dan eiwitten vouwen, en help mee ziekten als kanker en zo te bestrijden in de vrije tijd van je chip...
http://www.wetenscha...showtopic=59270
- Berichten: 3.135
Re: Warmtecapaciteit verzadigde lucht
Het gaat me om de grote lijn. Bedankt voor je hulp! 
Heb je interesse in journalistiek? Wij zoeken versterking! Speurwerk, deel van het team, meer weten: klik.